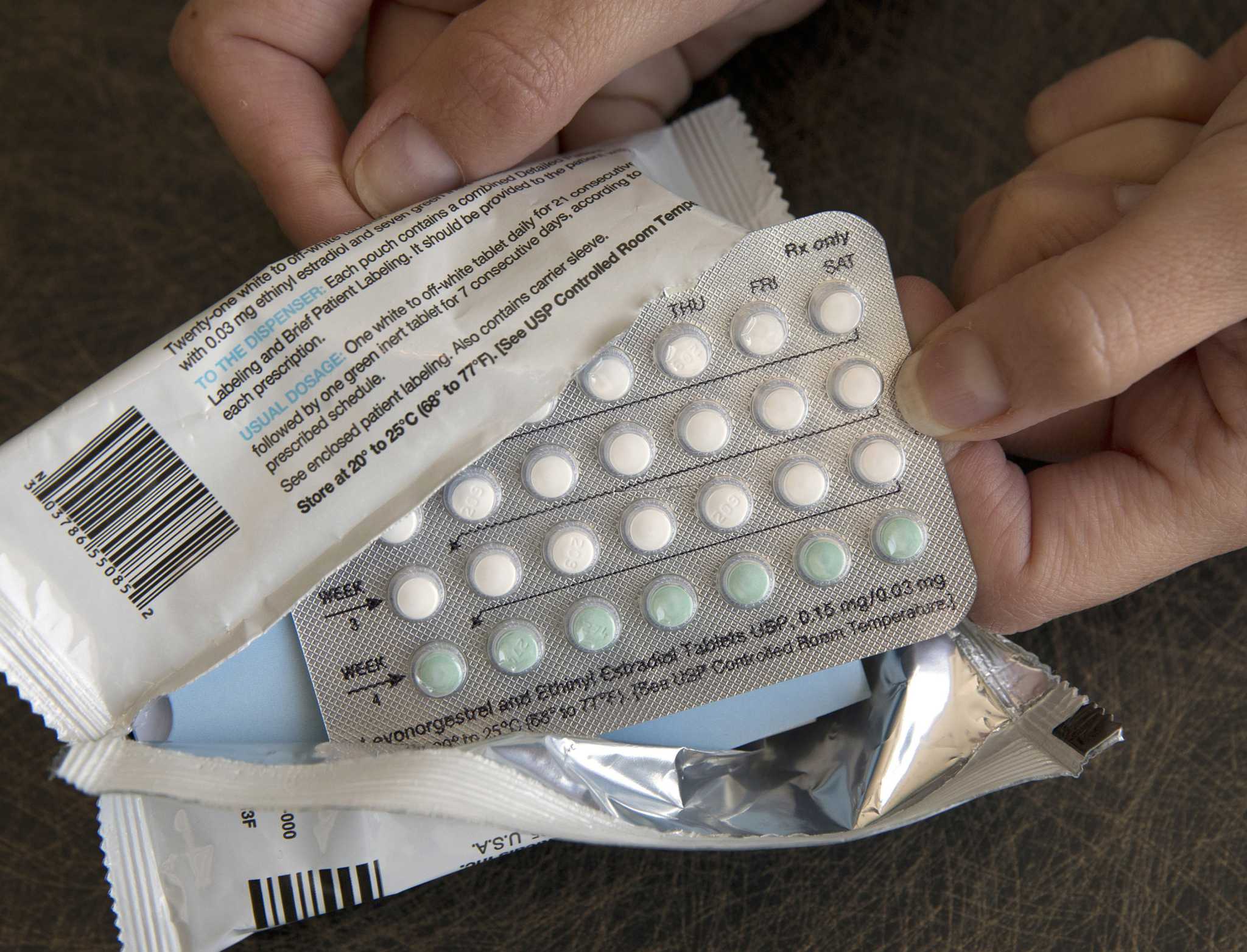
WASHINGTON (AP) – Por primera vez, una empresa farmacéutica ha pedido permiso para vender una píldora anticonceptiva sin receta en los Estados Unidos.
La solicitud de HRA Pharma el lunes establece una decisión de alto riesgo para los reguladores de salud en medio de batallas legales y políticas sobre la salud reproductiva de las mujeres. La empresa afirma que el momento no está relacionado con la reciente decisión del Tribunal Supremo de anular el caso Roe contra Wade.
Las píldoras hormonales han sido durante mucho tiempo la forma más común de control de la natalidad en los Estados Unidos, utilizadas por millones de mujeres desde la década de 1960. Siempre han requerido una prescripción, generalmente para que los profesionales de la salud puedan examinar las condiciones que aumentan el riesgo de coágulos sanguíneos raros, pero peligrosos.
La solicitud de la farmacéutica francesa recopila años de investigación con la intención de convencer a la Administración de Alimentos y Medicamentos de que las mujeres pueden examinarse a sí mismas para detectar esos riesgos y utilizar la píldora de forma eficaz.
“Para un producto que ha estado disponible durante los últimos 50 años, que ha sido utilizado con seguridad por millones de mujeres, pensamos que era el momento de hacerlo más accesible”, dijo Frederique Welgryn, directora de estrategia de HRA.
La aprobación de la FDA podría llegar el año que viene y sólo se aplicaría a la píldora de HRA, que se vendería bajo su marca original, Opill. La compañía adquirió el medicamento de décadas de antigüedad de Pfizer en 2014, pero actualmente no se comercializa en los Estados Unidos.
Los defensores de los derechos reproductivos quieren que otros anticonceptivos de prescripción pasen a ser de venta libre y, eventualmente, que las píldoras abortivas hagan lo mismo.
Esta posibilidad de sentar un precedente sitúa de nuevo a la FDA bajo un intenso foco político.
A finales del año pasado, la agencia fue condenada por los opositores al aborto y alabada por los defensores de los derechos de la mujer cuando flexibilizó el acceso a las píldoras abortivas. La agencia se enfrentó a presiones políticas similares en 2006 cuando aprobó el uso sin receta de la píldora anticonceptiva de emergencia Plan B.
Muchos grupos conservadores insisten en que sólo les interesa restringir el aborto, y las prohibiciones estatales suelen excluir explícitamente la anticoncepción.
Incluso antes del anuncio del lunes, los legisladores demócratas pedían a la FDA que considerara rápidamente cualquier solicitud de este tipo.
“Instamos a la FDA a que revise las solicitudes de píldoras anticonceptivas de venta libre sin demora y basándose únicamente en los datos”, dijeron más de 50 miembros del Caucus Pro-Choice de la Cámara de Representantes en una carta de marzo.
Muchos medicamentos comunes han salido del mostrador de la farmacia, incluidos los fármacos para aliviar el dolor, la acidez y las alergias.
En cada caso, las empresas deben demostrar que los consumidores pueden entender el etiquetado del medicamento, evaluar sus riesgos y utilizarlo de forma segura y eficaz sin supervisión profesional. La HRA dedicó siete años a realizar los estudios exigidos por la FDA, incluido un ensayo de seguimiento de 1.000 mujeres que tomaron su píldora durante seis meses.
Detrás de los esfuerzos de la empresa se encuentra una coalición de investigadores y defensores de la salud de la mujer que han trabajado durante casi dos décadas para que los anticonceptivos sean más accesibles, especialmente para los grupos con menos acceso a la atención sanitaria.
El Grupo de Trabajo sobre Anticonceptivos Orales de Venta Libre ayudó a financiar algunas de las investigaciones de la HRA y está movilizando apoyos en torno a una campaña mediática denominada Free the Pill.
“Gran parte de nuestra investigación ha consistido en exponer el caso para ayudar a inspirar y apoyar a una empresa para que asuma este trabajo”, dijo Kelly Blanchard, presidenta de Ibis Reproductive Health, un miembro del grupo que apoya el aborto y el acceso a los anticonceptivos.
Las píldoras anticonceptivas están disponibles sin receta en gran parte de Sudamérica, Asia y África. El año pasado, la empresa HRA, con sede en París, consiguió la aprobación en el Reino Unido de la primera píldora anticonceptiva disponible allí sin receta.
Los defensores del medicamento de HRA estaban especialmente interesados en él porque dicen que es probable que plantee menos problemas de seguridad.
La píldora contiene una única hormona sintética, la progestina, que impide el embarazo al bloquear los espermatozoides del cuello uterino.
La mayoría de las píldoras anticonceptivas contienen progestina más estrógeno, lo que puede ayudar a que los períodos sean más ligeros y regulares. Las píldoras con progestina se recomiendan generalmente a las mujeres que no pueden tomar las píldoras combinadas más populares debido a problemas de salud.
Pero el estrógeno también representa la mayor parte del riesgo de coágulos sanguíneos asociado a los anticonceptivos orales. El etiquetado de la FDA advierte contra su uso en ciertas mujeres que ya tienen riesgo de sufrir problemas cardíacos, como las que fuman y tienen más de 35 años.
Para la mayoría de las mujeres, los fármacos son abrumadoramente seguros. Según la FDA, de cada 10.000 mujeres que toman píldoras combinadas al año, entre tres y nueve sufren un coágulo de sangre.datos. Eso se compara con uno a cinco coágulos entre 10.000 mujeres que no toman anticonceptivos.
Y los profesionales médicos señalan que las tasas de coagulación son mucho más altas en las mujeres que se quedan embarazadas, cuando los niveles hormonales y la reducción del flujo sanguíneo aumentan el riesgo de coagulación.
“Lo que definitivamente veo es un malentendido de los peligros de estas píldoras. Es mucho más seguro tomar la píldora que quedarse embarazada”, dijo la Dra. Maura Quinlan, médico de la Universidad Northwestern y miembro del Colegio Americano de Obstetras y Ginecólogos. No participó en la solicitud ni en la investigación de la HRA.
La asociación médica es partidaria de que todos los anticonceptivos de base hormonal sean de venta libre. El mes pasado, la mayor agrupación de médicos del país, la Asociación Médica Americana, respaldó que las píldoras anticonceptivas puedan adquirirse sin receta.
Sin embargo, el apoyo no es universal.
Diana Zuckerman, del Centro Nacional de Investigación Sanitaria, sin ánimo de lucro, dice que comparar los riesgos de seguridad de las píldoras con el embarazo no es el enfoque correcto.
Muchas mujeres toman píldoras anticonceptivas para regular sus períodos o reducir el sangrado, dijo Zuckerman, cuyo grupo evalúa la investigación médica. “Esos son beneficios reales, pero no valen el riesgo de coágulos de sangre potencialmente mortales”, dijo.
La FDA lleva mucho tiempo vigilando la seguridad de los anticonceptivos orales, actualizando sus advertencias a lo largo de los años.
El año pasado, la agencia suspendió un estudio del fabricante de medicamentos Cadence Health, que también ha estado trabajando en una píldora de venta libre. La agencia pidió a la empresa que realizara controles adicionales de la presión arterial de los participantes en el ensayo. La empresa dice que “está trabajando para superar este obstáculo normativo”.
La FDA debe celebrar una reunión pública para evaluar la solicitud de HRA antes de tomar una decisión. Es probable que las consideraciones de seguridad ocupen el centro del escenario.
Los ejecutivos de HRA, que es propiedad de Perrigo Co., esperan una decisión en la primera mitad de 2023.
Los defensores esperan que sea la primera de muchas.
“Una vez que veamos la aprobación de este producto, se demostrará que es posible y que los datos son sólidos”, dijo Blanchard. “Con suerte, veremos cómo se acelera el proceso a partir de aquí”.
___
Siga a Matthew Perrone en Twitter: @AP_FDAwriter.
___
El Departamento de Salud y Ciencia de Associated Press recibe el apoyo del Departamento de Educación Científica del Instituto Médico Howard Hughes. La AP es la única responsable de todo el contenido.